[서울=뉴스핌] 박다영 기자 = 헬릭스미스가 당뇨병성 신경병증 유전자치료제 엔젠시스(VM202-DPN)의 임상 3상 과정에서 위약과 약물혼용을 의심하는 가운데, 임상 현장의 업무 담당자들은 "믿기 어려운 실수"라고 했다.
복수의 국내 제약사 임상 개발 업무 담당자들은 "여러 임상 현장에서 한 약물에 대해서만 대규모로 혼용이 일어나는 일은 흔치 않다"고 말했다.
 |
| [서울=뉴스핌] 박다영 기자 = 김선영 헬릭스미스 대표가 26일 서울 중구 프레스센터에서 기자간담회를 열고 임상 3상 결과와 향후 계획을 설명하고 있다. 2019.09.26 allzero@newspim.com |
헬릭스미스는 지난 23일 임상 3a상 결과 발표를 지연한다고 공시했다. 지연 이유는 VM202-DPN의 임상 3a상 과정에서 위약(가짜약)과 실험약이 뒤섞였기 때문이다. 대상자 477명 중 위약을 투여해야 할 환자군 중 최소 36명에서 엔젠시스가 검출됐고, 엔젠시스를 복용해야 할 환자군 중 32명 가량은 혈액에서 약물이 검출되지 않았다. 임상시험 대상자 중 14.2%에서 오류가 발생한 것이다.
헬릭스미스는 총 25개 병원에서 VM202-DPN의 임상 3상을 이중맹검 방식으로 진행했다. 이중맹검은 실험자와 피험자 모두 실제 변화가 이뤄지고 있는지 모르게 진행되는 방식이다.
김선영 대표는 지난 26일 기자간담회를 통해 "25개 병원 중 어떤 곳은 임상 대상자가 70명씩 있었고 어떤 병원은 5명 정도였다"며 "시스템이 체계적으로 잘 갖춰진 상위 3개 병원의 임상 대상자는 50~60명 정도인데, 여기서 임상을 진행한 경우는 통증 감소 효과의 통계적 유의미성을 의미하는 p값이 더 좋게 나왔다"며 환자 관리가 미흡한 일부 병원에서 약물 혼용이 발생했을 가능성을 시사했다.
임상 시험은 공장에서 완제의약품을 만들고 특정 기관이 약의 이름을 가린 채 병원에 분배하는 단계를 거쳐 진행된다. 병원에서 약물을 주사한 후에는 환자의 혈액을 채취해 임상수탁기관(CRO)에서 이를 분석한다.
이 과정 중 병원에서 발생할 수 있는 오류는 위약 조제 과정에서 착오나 의료진의 투약 실수, 데이터 오기재 등이다.
병원에서 담당자들은 착오나 실수가 발생할 수도 있지만, 한 임상시험에서만 10%가 넘는 표본에서 약물을 혼용한 오류가 생겼다는 사실은 믿기 어렵다고 봤다.
국내 제약사에서 임상 개발을 담당하는 A씨는 "병원 약사가 조제 중에 잘못 위약과 시험약을 바꿨다는 이야기를 들은 적 있다"면서 "하지만 1건에 불과했고, 이마저도 병원 약사들이 확인하는 과정에서 알아채고 폐기했다"고 했다.
그는 이어 "위약과 실험약이 구분하기 어려워 실수했다고 해도 10%가 넘을 정도로 대규모 표본에서 착오가 발생하는 일은 보지도, 듣지도 못했다"고 말했다.
투약 과정에서도 여러 병원에서 한 실수를 했을 가능성은 낮다고 봤다.
한 대학병원의 임상전문간호사 B씨는 "임상 투약은 정해진 과정에 따르기 때문에 병원 내에서 실수가 빚어지는 경우가 거의 없다"며 "사람이 하는 일이라 실수가 생겼다고 하더라도 25개 중 다수의 병원이 한 임상시험에 대해서만 동시다발적으로 같은 실수를 했을 확률은 거의 없다고 본다"고 말했다.
김경수 서울성모병원 임상시험센터장은 "임상시험이 이중맹검으로 디자인된 형태라면 조작이 원천적으로 불가능하다"라고 말했다.
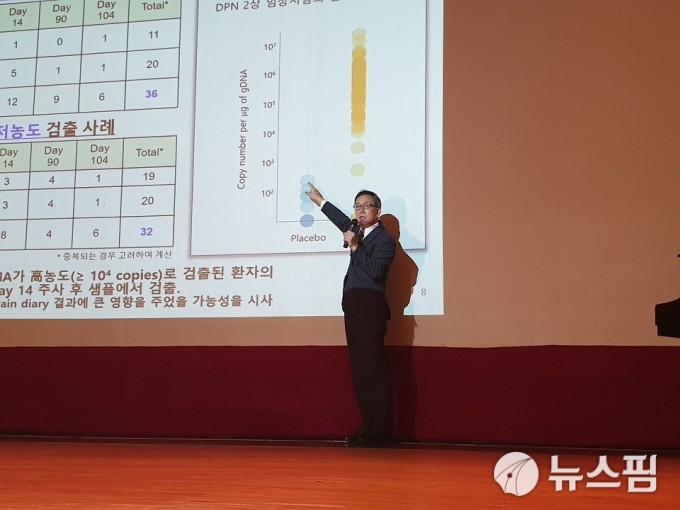 |
| [서울=뉴스핌] 박다영 기자 = 김선영 헬릭스미스 대표가 24일 서울 여의도동 NH투자증권에서 임상 3상 결과를 설명하고 있다. 2019.09.24 allzero@newspim.com |
다만, 헬릭스미스 측은 이 같은 약물 혼용은 충분히 있을 수 있다고 주장하고 있다.
김선영 헬릭스미스 대표는 26일 기자간담회를 열고 약물 혼용과 관련 "미국 식품의약국(FDA)에서는 신약 개발 과정에서 별의 별 사건이 다 있기 때문에, 저희와 같은 경우에 이미 상용화된 사례가 있을 것으로 생각된다"며 "이런 사례를 어떻게 방지하고 있는지 배울 것"이라고 했다.
allzero@newspim.com
 영상
영상