[편집자] 이 기사는 03월 22일 오전 09시48분 프리미엄 뉴스서비스'ANDA'에 먼저 출고됐습니다. 몽골어로 의형제를 뜻하는 'ANDA'는 국내 기업의 글로벌 성장과 도약, 독자 여러분의 성공적인 자산관리 동반자가 되겠다는 뉴스핌의 약속입니다.
[뉴스핌=김양섭 기자] 바이로메드가 미국서 '당뇨병성 신경병증 (VM202-DPN)' 치료제에 대한 피험자투여를 오는 2분기부터 시작하는 등 임상 3상을 본격화할 계획이다.
22일 바이로메드는 "VM202-DPN(당뇨병성 신경병증 치료제)은 2분기에 임상 3상 첫 피험자 투여를 계획하고 있다"고 밝혔다. 바이로메드는 미국에서 지난해 4월 이 치료제에 대한 3상 승인을 받은 바 있다. 바이로메드 관계자는 "그동안 준비작업을 거쳐 2분기에 피험자투여를 시작할 계획"이라고 설명했다.
임상단계는 일반적으로 1~3상 단계로 이뤄지며 1상은 안정성, 2상은 유효성, 3상은 대규모 피험자를 대상으로 종합적 검증을 하는 절차다. 이후 품목허가 등을 받은 뒤 상용화 단계에 들어서게 된다.
VM202-DPN은 손상된 미세혈관망과 신경세포의 재생을 유도하는 혁신적인 바이오 신약으로 알려져 있다.
VM202-DPN를 주사하면 투여부위에서 혈관생성과 신경성장을 유도하는 HGF 단백질이 생산된다. 이와 같이 만들어진 HGF 단백질은 당뇨병성 신경병증 환자들이 느끼는 극심한 통증을 치료할 수 있다. 이 같은 치료 효과는 미국과 한국에서 동시에 실시한 임상시험 1상과 2상을 통해 확인된 바 있다.
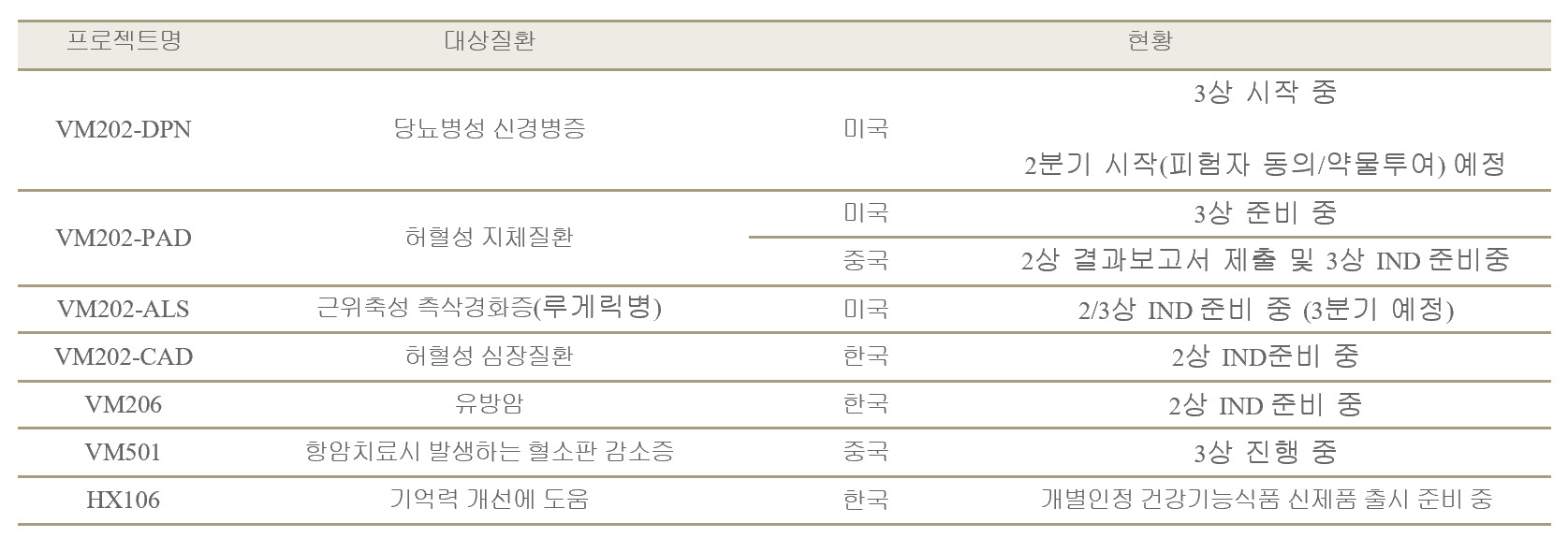
바이로메드는 VM202-DPN를 포함해 올해 미국에서 Pivotal 임상(품목허가를 받기 위한 3상 임상시험)을 3개 시작하는 계획을 갖고 있다. 루게릭병 치료제(VM202-ALS)에 대한 2/3상의 IND 신청을 진행할 계획이며, 당뇨병성 궤양을 대상으로 하는 VM202-PAD의 환자모집도 예정돼 있다.
아울러 글로벌 제약사로의 기술이전도 지속적으로 추진한다는 계획이다. 바이로메드측은 "VM202의 가치를 더 높이는 동시에 기술이전에서의 협상력을 강화시키기 위해 임상3상을 중단하거나 지연시키지 않고 신속하게 진행하는 것이 매우 중요하다고 판단했고, 이번 증자에 참여하며 개발 속도를 높이려 한다"고 밝혔다.
앞서 지난 18일 바이로메드는 약 150억원 규모의 제3자배정 유상증자 결정을 했다. 유상증자 대상은 김용수 대표와 최대주주인 김선영 씨다.
한편 바이로메드의 작년 실적은 매출 76억원, 영업이익 10억원, 당기순이익 2억5000만원이다. 지난해 초 5만원대이던 주가는 3월 이후 가파르게 오르기 시작해 연말 23만 900원까지(작년 12월 2일 장중고점) 상승했다. 이후 조정을 받아 최근 13만~17만원대 박스권에서 움직이고 있다. 21일 종가는 16만1900원이다.
[뉴스핌 Newspim] 김양섭 기자 (ssup825@newspim.com)
 영상
영상