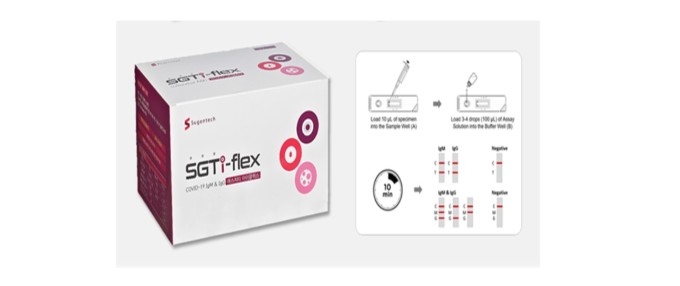
[서울=뉴스핌] 박다영 기자 = 수젠텍은 신종 코로나바이러스 감염증(코로나19) 항체진단키트 'SGTi-flex COVID-19 IgM/IgG'가 미국 식품의약국(FDA)에 제품등록(listing)을 완료했다고 6일 밝혔다. 제품등록을 통해 수젠텍은 미국 수출을 본격화할 전망이다.
코로나19 진단기기 FDA제품 등록은 '코로나19 긴급상황에 대비한 진단기기 제도'(Policy for Diagnostic Tests for Coronavirus Disease-2019 during the Public Health Emergency)가 도입되면서 본격화된 제도다. 미국 내 코로나19 확산히 급속하게 진행되면서 기존 분자진단(PCR) 키트 외에 항체진단키트도 제품등록을 완료하면 각 주에서 자유롭게 사용할 수 있다.
수젠텍 관계자는 "미국에 진단키트 공급이 가능하도록 FDA의 공식인증을 받는 방식은 FDA 긴급사용승인(EUA)을 받거나 제품등록(listing)을 하는 2가지가 있다"며 "수젠텍이 개발한 항체 신속진단키트는 긴급사용승인보다 제품등록(listing)을 하면 더 빠르게 공급이 가능하기 때문에 FDA 제품등록을 우선 추진했다"고 밝혔다.
수젠텍의 SGTi-flex COVID-19 IgG/IgM은 2개 항체(lgG, lgM)를 동시에 진단하는 방식으로 코로나19 감염 여부를 확인한다. 피 한 방울을 키트에 떨어뜨리면 10분내 코로나19 환자인지 진단한다.
현재 국내에서는 코로나19 감염여부를 확인하는 진단 키트로 분자진단키트를 활용하고 있다. 감염전문가들은 항체진단키트의 검사 시간은 짧지만 정확도가 50~70% 정도로 분자진단키트에 비해 낮은 것으로 판단하고 있다. 분자진단키트는 정확성이 90% 이상이지만, 진단을 위해 전문검사 시설과 장비, 임상병리사 등을 갖춰야 한다.
미국 FDA는 기존에 분자진단키트만 긴급사용승인(EUA)을 내줬지만, 이달초부터 급증하는 진단 수요를 충족하기 위해 항체신속진단키트에 대해서도 긴급사용승인을 내주기 시작했다.
수젠텍 관계자는 "이미 미국 주요 3개 주정부와 제품공급을 협의중이고 미국 대기업에도 샘플을 공급해 테스트 절차를 진행중"이라며 "유럽, 아시아 지역과 미국에서 공급 요청이 쇄도하고 있어 공급 물량을 늘이기 위해 노력중"이라고 말했다.
그는 이어 "이번달 중순부터 생산량을 현재의 5배로 늘리고, 5월부터는 다시 2배를 늘릴 예정으로 미국 공급도 가능할 전망"이라며 "제품등록에 이어 긴급사용승인과 관련해 FDA와 논의가 진행 중"이라고 설명했다.
allzero@newspim.com
 영상
영상