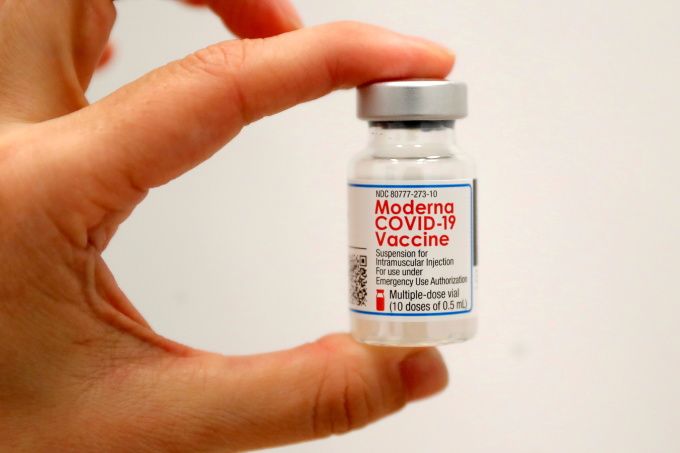
[서울=뉴스핌] 김경민 기자 = 미국 제약사 모더나의 신종 코로나바이러스 감염증(코로나19) 백신 '모더나코비드-19백신주'가 국내 유통 허가를 위한 마지막 검증 절차만을 남겨뒀다. 관련 업계에서는 모더나 백신의 유통 허가가 날 가능성이 높다고 전망하고 있다.
17일 식품의약품안전처(식약처)에 따르면 오는 21일 최종점검위원회(최종점검위)를 열고 GC녹십자가 수입품목허가를 신청한 모더나 백신 허가 여부를 결정할 예정이다.
식약처는 객관적이고 투명한 허가·심사를 위해 코로나19 백신과 치료제의 경우 안전성·효과성 검증 자문단(검증 자문단)→중앙약사심의위원회(중앙약심)→최종점검위 등 외부 전문가 3중 자문 절차를 거치도록 하고 있다.
앞서 지난 9일 열린 검증 자문단 회의에서 전문가들은 모더나 백신의 임상시험 3상 결과를 보고 예방 효과가 94.1%로 허가 가능한 수준이라고 판단했다. 백신 투여군에서 중증 환자나 코로나19로 사망한 사례도 없었다.
지난 13일 일린 중앙약심 회의에서도 모더나 코로나19 백신의 안전성과 효과성 등을 검토하고 품목허가가 가능하다는 결론이 나왔다. 다만 전문가들은 허가 후 전반적인 안전성 확보를 위해 '위해성관리계획'이 필요하다고 의견을 보탰다.
식약처는 검증 자문단과 중앙약심의 자문을 통해 얻은 전문가 의견 등을 종합해 모더나 백신의 품질 자료 등 추가 제출 자료를 검토한 뒤 최종점검위에서 판단을 내릴 계획이다.
모더나 백신의 안전성 등은 이미 해외에서 검증된데다 마지막 절차인 만큼 유통 허가가 날 가능성을 높게 내다보고 있다. GC녹십자가 신청한 모더나 백신은 지난해 12월 미국과 지난 1월 영국 등에서 긴급사용을 승인한 백신이다. 또 유럽연합(EU)과 캐나다, 스위스에서는 허가 후 자료를 추가로 제출하도록 조건부 허가를 한 상황이다.
김우주 고려대 구로병원 감염내과 교수는 "(허가에) 별 문제 없을 것 같다"며 "미국에서 임상시험 3상을 통해 안전성이 입증됐고, 효능이나 안전성에도 크게 문제가 없다는 결과가 나왔다"고 말했다.
관련 업계 관계자 역시 "선진국에서도 안전성, 효과성에 대해 인정하고 긴급사용을 승인했다"며 "이변이 없는 한 허가가 날 확률이 크다고 예상한다"고 했다.
모더나 백신은 28일 간격을 두고 2회 투여하는 용법으로 개발됐다. 이 백신은 화이자 백신과 마찬가지로 코로나19 바이러스의 유전자(mRNA)를 미세한 입자에 담아 체내로 주입해 면역 반응을 유도하는 원리다.
kmkim@newspim.com
 영상
영상