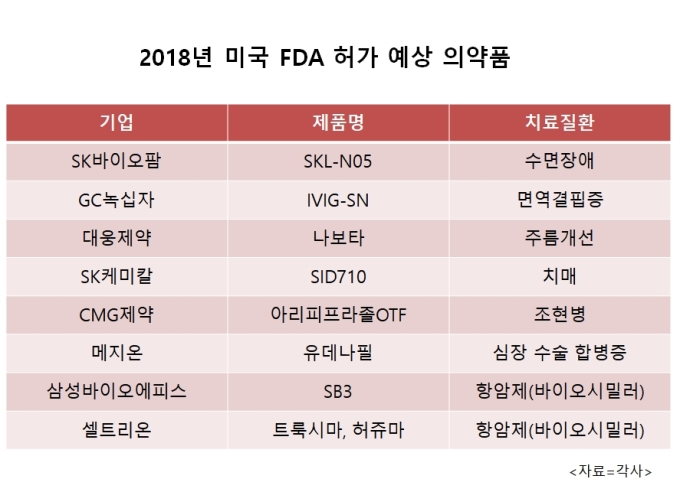
[뉴스핌=김근희 기자] 올해 국내 제약·바이오 업체들이 세계 최대 의약품 시장인 미국을 정조준한다. 약 9개의 국산 의약품이 올해 미국 식품의약국(FDA)의 판매 승인을 받을 것으로 보인다. 이는 역대 최대다. 한미약품, SK바이오팜 등 올해 미국 판매 허가 신청을 계획 중인 기업들도 줄을 서 있다.
◆9개 의약품 美 판매 승인 기대
6일 관련 업계에 따르면 미국 FDA는 최근 SK바이오팜의 수면장애 치료제 'SKL-N05'의 판매 허가 신청 접수를 마치고, 검토를 시작했다. SKL-N05는 SK바이오팜과 수면장애 질환 시장 1위 제약사인 미국의 재즈가 공동개발 중인 치료제다.
SK바이오팜은 이르면 올해 판매허가를 받고, 내년 초 미국에 제품을 출시할 것으로 보인다. 통상적으로 판매 허가가 나오기까지 10개월이 걸리기 때문이다.
업계에서는 SKL-N05를 포함해 올해 총 9개의 국산 의약품들이 FDA 판매 허가를 받을 것으로 예상하고 있다. GC녹십자, 대웅제약, 셀트리온, 삼성바이오에피스 등이 FDA 판매 허가를 기다리고 있다.
GC녹십자는 올해 3분기 이내에 면역결핍 치료제 '아이비글로불린-에스엔(IVIG-SN)의 미국 판매 허가를 받을 것으로 보인다. 회사는 2013년 FDA에 판매 허가를 신청했으나 2016년 FDA로부터 제조 공정 관련 자료의 보완이 필요하다는 공문을 받았다. 부족한 부분을 보완한 만큼 올해 시판허가가 유력하다는 것이 업계의 관측이다.
바이오시밀러(바이오의약품 복제약) 기업 셀트리온은 지난해 6~7월 FDA에 혈액암 치료제 '트룩시마'와 유방암 치료제 '허쥬마'의 판매 허가를 신청했다. 지난해 말 유방암 치료제 'SB3'의 판매 허가를 신청한 삼성바이오에피스도 결과를 기다리는 중이다.
대웅제약은 지난해 FDA로부터 보툴리눔 톡신(보톡스) '나보타' 제2공장 실사를 받았다. 대웅제약 관계자는 "지난달 FDA가 무균시설 결함 등을 보완할 것을 주문했으나 심각한 문제는 없었다"고 말했다. 이르면 올해 판매허가가 날 것이란 전망이 나온다.
◆美, 세계 최대 의약품 시장…도전 계속
이처럼 국내 제약·바이오 업체들의 미국 진출은 탄력을 받고 있다. LG화학의 항생제 '팩티브'가 처음 미국 시장에 출시된 2003 이후 지난해까지 미국에 출시된 한국 의약품이 9개에 불과하다는 점에서 의미가 남다르다.
특히 미국은 한국 제약·바이오 업체들이 세계적 기업으로 도약하기 위해서 꼭 거쳐야 할 시장이다. 의약품 시장의 규모가 전 세계에서 가장 크기 때문이다. 시장조사기관 IMS헬스에 따르면 2015년 기준 미국 의약품 시장 규모는 4300억달러(약 462조)로 전 세계 시장의 40.2%를 차지한다.
업계 관계자는 "9개 국산 의약품의 미국 시장 진출이 다가왔다는 것은 그만큼 한국 제약·바이오 기술 수준이 높아졌다는 것"이라며 "판매허가 이후에도 미국 시장에서 살아남기 위한 전략을 짜야 한다"고 말했다.
올해도 한국 제약·바이오 업체들은 계속해서 미국 시장의 문을 두드릴 예정이다.
대웅제약은 올 하반기 FDA에 대표제품인 '우루사'의 판매허가를 신청할 방침이다. 회사는 현재 이를 위해 캐나다에서 우루사의 생물학적 동등성 시험을 진행하고 있다.
SK바이오팜도 올 하반기 뇌전증 치료제 '세노바메이트'의 미국 판매 허가 신청을 계획 중이다. 한미약품은 오는 4분기 지속형 호중구감소증 치료제 '롤론티스'의 미국 진출에 도전한다.
[뉴스핌 Newspim] 김근희 기자 (keun@newspim.com)
 영상
영상