[서울=뉴스핌] 김근희 기자 = 앞으로 희귀질환 신약의 경우 임상시험 계획 승인만 받아도 희귀의약품 지정이 가능해진다.
식품의약품안전처(처장 류영진)는 이 같은 내용을 담은 '희귀의약품 지정에 관한 규정' 개정안을 행정예고했다고 18일 발표했다.
희귀의약품은 희귀질환이나 암과 같이 적절한 대체의약품이 없고, 환자들에게 긴급하게 필요한 의약품을 뜻한다. 희귀의약품에 지정된 경우 임상시험 2상만 마쳐도 조건부로 우선 판매 허가를 받을 수 있다.
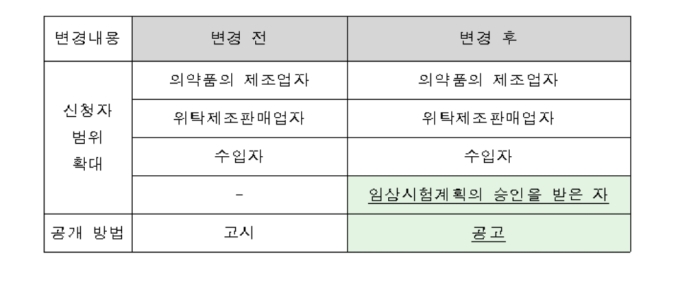
그동안 의약품 제조업, 위탁제조판매업, 수입자만 희귀의약품으로 지정받아 제품을 개발할 수 있었다. 또 행정예고 등을 거쳐야만 희귀의약품에 지정될 수 있었다.
그러나 이번 개정안을 통해 임상시험 계획을 승인 받은 경우에도 희귀의약품 지정 신청이 가능하게됐다. 희귀의약품 지정도 식약처 홈페이지를 통해 공고되는 등 기간이 단축된다.
식약처 관계자는 "이번 개정안이 희귀의약품의 개발·공급 확대에 도움이 될 것"이라며 "앞으로도 희귀·난치질환자의 치료 기회 보장을 위해 정책적 지원을 지속해 나겠다"고 말했다.
keun@newspim.com
 영상
영상