[서울=뉴스핌] 박효주 기자 = 필립모리스 인터내셔널(PMI)이 식품의약품안전처의 궐련형 전자담배 연구 결과를 정면 반박하는 결과를 발표했다.
18일 필립모리스 인터내셔널은 서울 중구 포시즌호텔에서 기자간담회를 열고 궐련형 전자담배 아이코스는 임상시험 결과를 발표했다.
이번 대규모 임상연구는 미국에서 약 1000명의 흡연자를 일반담배 흡연자와 아이코스로 전환한 사용자 등 두 그룹으로 나눠서 이들의 신체 반응을 6개월 동안 측정했다.
그 결과 아이코스로 전환 흡연자는 6개월 후 8가지 신체평가지표(주요 임상위험 평가지표)가 모두 개선된 것으로 나타났다.
마누엘 피취(Manuel Peitsch) PMI 과학연구 최고책임자박사는 “이번 아이코스 연구 결과는 매우 고무적”이라며 “이는 연기 없는 제품의 위험도 감소 가능성을 직접적으로 평가한 최초의 대규모 임상연구다. 이번 연구 결과로 일반담배 흡연에 비해 아이코스로 전환하는 것이 담배의 위험도를 줄인다는 것을 증명할 수 있는 이정표를 마련했다”고 밝혔다.
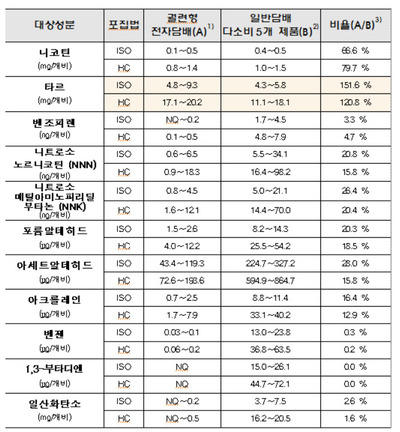
이번 필립모리스 연구결과는 최근 식약처 분석과 차이를 보인다. 특히 식약처는 궐련형 전자담배 분석 결과 중 일부 궐련형 전자담배의 경우 타르 수치가 일반담배에 비해 높다고 밝혀 논란이 커졌다.
타르 수치는 잔여물의 단순 무게(mg)이므로 독성물질과 그렇지 않은 잔여물이 어떻게 구성돼 있는지를 보여주지 못한다는게 회사 측 설명이다.
김병철 한국필립모리스 전무는 “더 이상의 혼란을 막기 위해서라도 식약처는 이미 궐련형 전자담배로 전환한 분들이나 앞으로 이를 고려하는 흡연자들에게 궐련형 전자담배의 유해물질이 일반담배 대비 현저히 감소했다는 사실을 명확히 밝혀야 할 것”이라며 “흡연자들에게는 정확한 정보를 제공 받을 권리가 있다”고 말했다.
한국필립모리스는 최근 복지부가 발표한 궐련형 전자담배 경고그림에 대한 우려도 표했다.
궐련형 전자담배의 위해성 감소에 대한 과학적 증거가 제출되고 있는 만큼 상대적인 위험도 차이를 소비자가 인지할 수 있어야한다는 주장이다.
한편 이번 임상시험 연구 결과는 지난 8일 ‘위험감소담배제품(MRTP)’과 판매 승인을 검토 중인 미국 식품의약국(FDA)에 제출됐고 조만간 식품의약품안전처를 비롯한 국내 관련 부처에도 제출될 예정이다.
hj0308@newspim.com
 영상
영상