[서울=뉴스핌] 김근희 기자 = 바이오시밀러(바이오의약품 복제약) 시장이 성장하면서 '퍼스트무버' 경쟁도 치열해지고 있다. 가장 먼저 바이오시밀러를 출시해 시장을 선점하기 위해서다. 특히 셀트리온과 삼성바이오에피스 등은 미국과 유럽 등에서 두각을 나타내고 있다.
◆ 셀트리온 '트룩시마', 사실상 미국 시판 허가
12일 업계에 따르면 셀트리온의 혈액암용 바이오시밀러 '트룩시마'가 사실상 미국 판매 허가를 받았다. 미국 식품의약국(FDA) 항암제 자문위원회는 만장일치로 트룩시마 승인 권고를 내렸다. 이에 따라 연내 정식 허가가 나올 것으로 보인다.
정식 허가를 받으면 트룩시마는 미국 시장에 나오는 첫 '리툭산'(성분명 리툭시맙) 바이오시밀러가 된다. 지난해 산도스가 FDA에 리툭산 바이오시밀러 허가를 신청했고, 화이자, 암젠, 삼성바이오에피스 등은 임상시험을 진행 중이다.
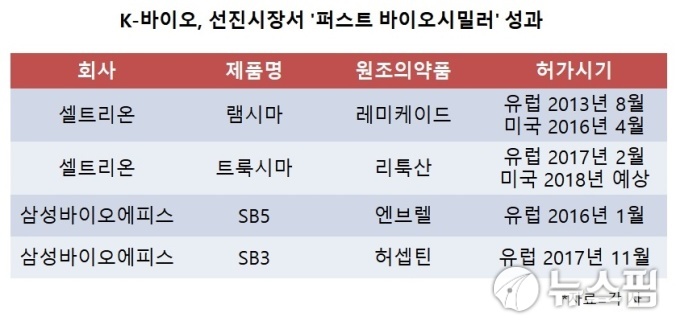
셀트리온은 계속해서 퍼스트 바이오시밀러를 내놓고 있다. 2013년 8월에는 자가면역질환 치료제 '레미케이드'의 바이오시밀러 '램시마'의 유럽 판매허가를 세계 최초로 받았다. 2016년에는 램시마의 미국 승인을 처음으로 받았다. 지난해 2월에는 트룩시마 유럽 승인을 받았다.
삼성바이오에피스도 자가면역질환치료제 '엔브렐'과 유방암 치료제 '허셉틴' 바이오시밀러인 브렌시스(SB5), 샴페넷(SB3)을 유럽에서 가장 먼저 승인받았다.
셀트리온 관계자는 "의약품 시장은 선점 효과가 중요한 만큼 첫 바이오시밀러라는 지위가 유리하게 작용한다"며 "트룩시마의 출시 시기는 판매를 담당하는 테바 등과 전략적으로 결정할 것"이라고 말했다.
◆ 바이오시밀러 경쟁 심화… 선별 전략도 필요
다만, 업계에서는 바이오시밀러 경쟁이 치열하지는 만큼 속도전 외에도 다른 전략도 중요해지고 있다는 분석이 나온다.
화이자, 산도스, 암젠 등 다국적 제약사들도 레미케이드 바이오시밀러 개발에 나섰고, 산도스는 유럽에서 리툭산 바이오시밀러 허가를 받았다.
업계 관계자는 "바이오시밀러의 시장 진입 시기도 중요하지만, 경쟁자가 적은 바이오시밀러를 찾아 이를 개발하는 것도 고려해야할 사항"이라고 말했다.
최근 다국적 제약사 MSD(미국 머크)가 당뇨병 치료용 바이오시밀러 '루수두나' 상업화 계획을 취소한 것도 이러한 시장 변화 때문으로 보인다.
당뇨병 치료제 '란투스'의 바이오시밀러인 루수두나는 MSD가 개발과 상업화를, 삼성바이오에피스가 공동 투자를 한 의약품이다. 란투스 바이오시밀러 시장은 이미 베링거인겔하임, 리리 등이 선점하고 있다.
MSD가 상업화를 포기하면서 삼성바이오에피스는 MSD로부터 투자보상금 등 1755억원을 받게 된다. 삼성바이오에피스는 이를 연구·개발(R&D)에 투자해 후속 파이프라인 개발에 박차를 가할 것으로 보인다.
keun@newspim.com
 영상
영상