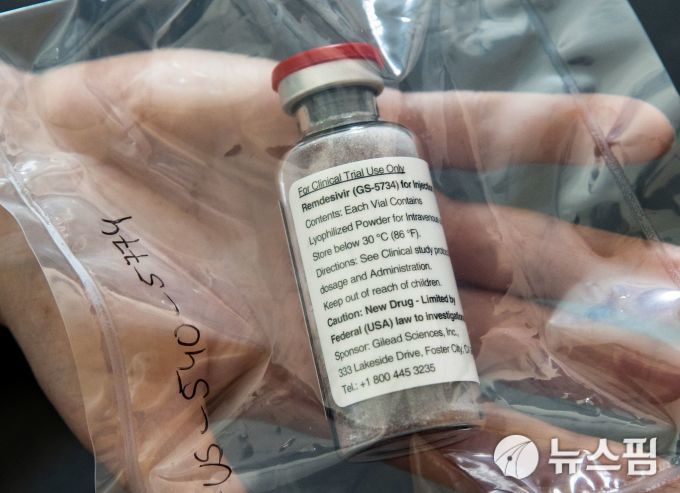
[서울=뉴스핌] 오영상 전문기자 = 일본 정부가 이번 주 내로 렘데시비르 판매를 승인해 이달 중에는 의료 현장에서 사용이 가능해질 전망이라고 4일 니혼게이자이신문 등이 보도했다.
보도에 따르면 길리어드 사이언스의 일본법인은 이날 후생노동성에 렘데시비르의 제조·판매 승인을 신청했다. 코로나19 치료약으로서는 일본 내 첫 승인 신청이다.
후생노동성은 이번 주 내로 승인 결정을 내려 이달 중 현장에서 사용할 수 있도록 한다는 방침이다. 이를 위해 일본 정부는 지난 2일, 렘데시비르의 특례 승인을 위한 의약품의료기기법 시행령을 개정했다.
특례 승인 제도는 긴급성이 높은 의약품에 대한 심사 절차를 대폭 간소화해 통상 1년이 걸리는 기간을 대폭 단축할 수 있다는 장점이 있다.
단, △국민 건강에 중대한 영향을 미칠 우려가 있는 병의 만연 방지에 필요하고 △다른 치료약이 없는 경우 △일본과 같은 수준의 승인 제도가 있는 나라에서 판매되는 것 등의 조건을 충족해야 한다.
일본 정부는 일본과 같은 수준의 승인 제도가 있는 나라로서 미국 등 5개국을 지정했다. 앞서 미국 식품의약국(FDA)은 지난 1일 코로나19 치료약으로서 렘데시비르의 사용을 승인했다.
NHK는 2일 "렘데시비르가 승인될 경우 일본 내 첫 코로나19 치료제가 된다"면서 "하지만 공급량이 제한돼 있어 당분간은 특정 병원에만 공급될 가능성이 있다"고 전했다.
goldendog@newspim.com
 영상
영상