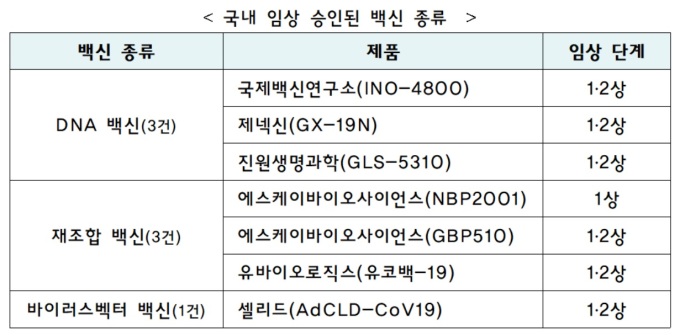
[서울=뉴스핌] 서영욱 기자 = 식품의약품안전처는 신종 코로나바이러스 감염증(코로나19)의 국내 백신 '유코백-19'의 임상시험계획을 승인했다고 21일 밝혔다. 제조사는 유바이오로직스다.
이에 따라 현재 국내에서 코로나19 관련 임상시험계획을 승인받아 개발을 진행하고 있는 의약품은 백신 7개 제품, 치료제 15개 제품으로 늘었다.
이번 임상시험에서 건강한 성인을 대상으로 '유코백-19'의 안전성과 면역원성(바이러스 감염성을 없애거나 낮추는 중화항체 증가 비율)을 평가한다. 1상 진행 후 2상을 순차적으로 진행한다.
'유코백-19'는 코로나19 바이러스의 '표면항원 단백질'을 유전자 재조합 기술을 이용해 만든 '재조합 백신'이다.
백신의 표면항원 단백질이 면역세포를 자극해 중화항체를 형성하고 코로나19 바이러스가 침입하면 항체가 코로나19 바이러스를 제거하는 원리다. 해외에서도 미국 노바백스 등 유전자재조합 기술을 이용한 코로나19 백신의 임상시험을 진행하고 있다.
식약처 관계자는 "코로나19 치료제·백신 개발에 대한 국민적 관심이 높은 점 등을 고려해 개발 제품의 임상시험 현황에 대한 정보를 신속하게 전달하겠다"며 "안전하고 효과 있는 코로나19 치료제·백신이 신속히 개발될 수 있도록 지원하겠다"고 말했다.
syu@newspim.com
 영상
영상