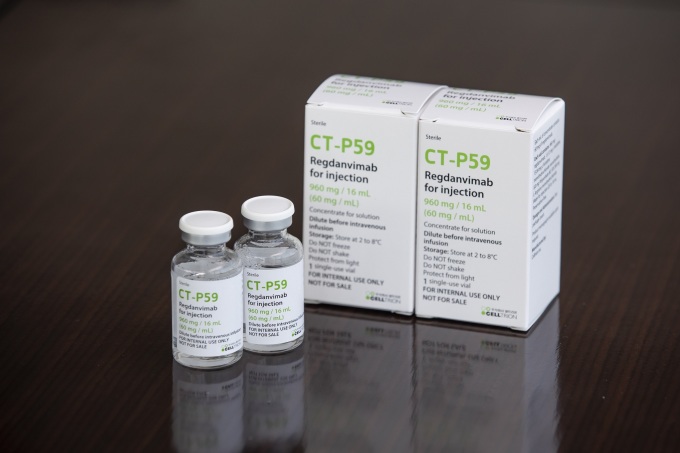
[서울=뉴스핌] 박다영 기자 = 셀트리온의 신종 코로나바이러스 감염증(코로나19) 항체치료제 '렉키로나주'(성분명 레그단비맙)의 조건부 허가 여부가 오늘 결정된다. 오늘 조건부 허가를 승인받으면 렉키로나주는 최초 국산 치료제가 된다.
식품의약품안전처는 5일 오전 10시 식약처 브리핑실에서 렉키로나주의 임상 2상 결과 안전성과 효능을 검증하는 마지막 관문인 '최종점검위원회' 회의를 진행한다. 회의 결과는 오후 2시 브리핑을 통해 발표한다.
조건부 허가는 치료제가 없는 질환에 대해 임상 3상을 진행하는 조건하에 임상 2상 결과로 판매 허가를 내주는 제도다. 식약처는 코로나19 치료제에 대해 검증 자문단, 중앙약사심의위원회(중앙약심), 최종점검위원회 등 3단계의 전문가 자문 단계를 거쳐 조건부 허가 여부를 결정한다.
렉키로나주는 앞서 두 단계에서 임상 3상을 진행하는 조건하에 품목허가 승인이 가능하다는 권고 의견을 받았다.
임상 2상 결과 위약(가짜약) 투여군과 비교했을 때 렉키로나주를 투여받은 환자는 입원 치료가 필요한 중증환자 발생률이 54% 낮고, 코로나19 증상 회복까지 걸리는 기간이 3.43일 빠른 것으로 나타났다.
이 데이터를 두고 검증자문단은 코로나19 증상 개선 시간 단축이 통계적 유의성이 있는 것이라고 판단하고 코로나19 경증 및 중등증 환자에 투여할 수 있다고 봤다.
전문가 자문 2단계인 중앙약심에서는 경증 환자에서 통계적으로 유의한 수준의 치료 효과를 확인하기 어렵다는 분석이 나왔다. 경증 환자는 고위험군 경증 환자로 좁혀 투약해야 한다고 자문했다.
관련 업계에서는 렉키로나주가 외부 전문가 자문 두 단계에서 잇따라 조건부 허가 권고 의견을 받은 만큼, 오늘 최종점검위원회도 무리 없이 통과할 수 있을 것으로 보고 있다. 업계 관계자는 "이미 두 단계를 거쳐 전문가들이 조건부 허가를 받아도 좋다는 권고 의견을 냈는데 이를 뒤집는 결과가 나오긴 어렵지 않을까 생각한다"고 말했다.
다만, 감염병 전문가들 사이에서는 항체 치료제가 '게임 체인저'가 되기는 어렵다는 전망이 나온다. 임상시험 연구 방법과 설계가 제대로 공개되지 않았고, 변이 바이러스에는 오히려 역효과가 나타날 수 있다는 이유에서다.
김우주 고려대 구로병원 감염내과 교수는 "렉키로나주의 임상 설계가 제대로 공개되지 않았고, 남아공, 브라질에서 나타난 변이 바이러스에 대한 항체 결합력도 확인되지 않았다"고 우려했다.
방지환 국립중앙의료원 중앙감염병병원운영센터장은 온라인 토론회에서 "코로나19 바이러스가 변이돼 스파이크 단백질의 구조가 달라질 경우, 변이 바이러스와 애매하게 결합해 세포 침투와 증식을 도울 수도 있다"고 말했다.
셀트리온은 조건부 허가를 전제하고 코로나19 환자 10만명에 투약할 수 있는 렉키로나제 생산을 마친 상태다. 내년에는 150~200만명분의 치료제를 생산할 계획이다.
허가를 받으면 렉키로나주를 국내에 원가로 공급할 계획이다. 미국에서 긴급사용승인을 받은 릴리와 리제네론의 코로나19 항체치료제는 1회 투여량 가격이 100만원을 웃도는 것으로 알려져 있다. 렉키로나주 1인 투여분의 원가는 40만원 선으로 알려졌다. 국내 환자들은 무료로 투약받게 될 것으로 보인다.
셀트리온 관계자는 "10만명 분 생산을 마쳐 허가되면 바로 출시할 수 있다"며 "해외 승인 절차도 추진 중"이라고 말했다.
allzero@newspim.com
 영상
영상