[서울=뉴스핌] 김근희 기자 = 국내 제약·바이오 업체들이 난치병 환자들을 위한 희귀의약품 개발에 나서고 있다. 조건부 허가, 세금 감면 등의 혜택을 얻을 수 있는 데다 절대 강자가 없는 틈새시장이기 때문이다.
희귀의약품이란 환자 수가 적고, 적절한 대체의약품이 없어 긴급한 도입이 필요한 의약품을 뜻한다. 미국에서는 환자 수 20만명 이하인 질환, 국내에선 환자 수 2만명 이하인 질환을 희귀질환으로 분류한다.
◆제약·바이오 社, 잇단 희귀의약품 지정
24일 관련 업계에 따르면 국내 제약·바이오 업체들이 잇따라 미국 식품의약국(FDA)으로부터 희귀의약품 지정(ODD)을 받고 있다. 희귀의약품 지정은 희귀난치성 질병 또는 생명을 위협하는 질병의 치료제 개발 및 허가를 지원하는 제도다.
이달 FDA는 한미약품의 '오락솔'을 혈관 육종 치료를 위한 희귀의약품으로 지정했다. 오락솔은 주사용 항암제를 먹는 제형으로 바꾼 치료제로, 2011년 미국 바이오 기업인 아테넥스에 기술이전됐다.
한미약품은 앞서 지난 2월에도 FDA로부터 선천성 고인슐린증 치료제 '랩스글루카곤 아날로그'를 희귀의약품으로 지정받았다.
영진약품이 지난해 스웨덴 기업에 기술이전 한 유전성 미토콘드리아 호흡계질환 치료제(KL1333)도 이달 희귀의약품으로 지정됐다. 이외에도 바이오리더스, 크리스탈지노믹스, 파멥신 등 바이오 업체들이 개발하고 있는 신약들이 FDA의 희귀의약품으로 지정받았다.
◆"허가 혜택은 늘고, 개발 비용은 줄고"
한미약품 등 국내 업체들은 희귀의약품 지정을 받음에 따라 앞으로 세금감면, 허가신청 비용 면제 등의 혜택을 받는다. 특정 희귀질환을 치료하는 최초의 의약품일 경우에는 7년간 시장 독점권이 인정된다.
국내 업체들이 희귀의약품 개발에 나서는 것은 바로 이러한 혜택 때문이다. 희귀질환 환자들을 위해 미국뿐 아니라 각국 정부가 희귀의약품 개발 기업에 다양한 혜택을 지원하고 있다.
한국의 식품의약품안전처의 경우에는 희귀의약품만 조건부 허가를 내준다. 조건부 허가는 임상시험 2상만 마쳐도 먼저 판매허가를 내주는 제도다.
연구·개발(R&D) 투자 규모가 작고, 상대적으로 인지도가 낮은 국내 업체들에는 유리한 조건인 셈이다.
생명공학정책연구센터 관계자는 "희귀의약품은 그동안 환자가 적어 시장성이 낮게 평가됐다"며 "그러나 국가 차원의 강력한 지원정책, 제약사들의 적응증을 확대 전략 등에 힘입어 관련 시장이 유망할 것으로 전망한다"고 말했다.
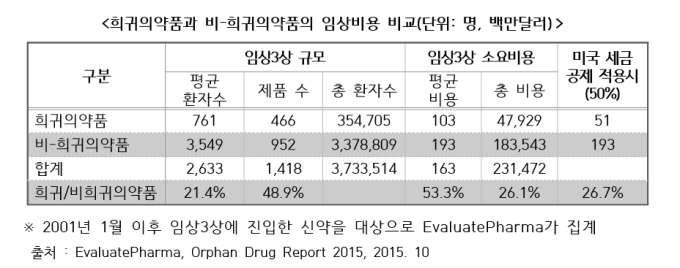
환자 수가 적어 R&D 비용이 적게 든다는 것도 희귀의약품 개발의 이점이다. 임상시험에서 모집해야할 환자 수가 다른 질병에 비해 적다. 다만, 환자수 모집이 어렵다는 단점이 있다.
생명공학정책연구센터에 따르면 희귀의약품 임상 3상에 드는 비용은 다른 치료제 임상시험 3상 비용의 절반에 불과하다.미국 정부가 희귀의약품에 한해 세금을 감면해준다는 것을 고려하면 비용은 4분의 1로 줄어든다.
◆2020년 희귀의약품 시장 규모 191조원
희귀의약품 시장은 성장성은 있지만, 경쟁은 상대적으로 덜한 시장이다. 환자 수가 적고, 기존 치료제가 없어 다국적 제약사들과 경쟁할 가능성이 작다.
업계 관계자는 "희귀의약품 시장은 다국적 제약사와 같은 절대 강자가 적은 틈새시장"이라며 "상대적으로 규모가 작은 국내 기업들도 수월하게 시장에 진입할 수 있다"고 설명했다.
또 희귀의약품 시장은 계속 성장 중이다. 제약산업 분석업체 '이밸류에이트 파마(EvaluatePharma)에 따르면 희귀의약품 세계 시장 규모는 2015년 1030억달러(약 110조원)에서 2020년 1780억달러(약 191조원)규모에 이를 것으로 추산된다.
keun@newspim.com
 영상
영상