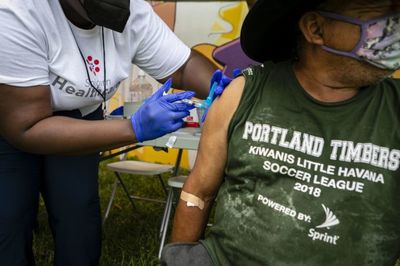
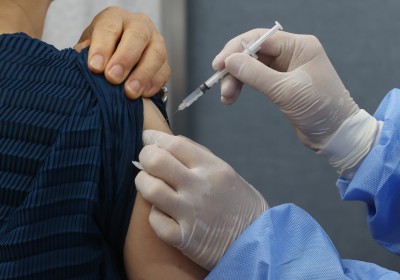
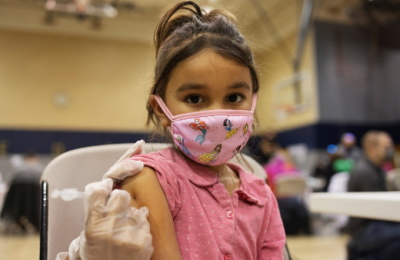
[서울=뉴스핌] 방보경 기자 = SK바이오사이언스의 코로나19 백신이 첫 해외 승인 획득에 성공했다.
SK바이오사이언스는 코로나19 백신 '스카이코비원(유럽명 스카이코비온)'이 영국 의약품 규제당국(MHRA)으로부터 영국, 스코틀랜드, 웨일즈 지역에서 18세 이상 성인에 대한 기초 접종(1,2차)용 정식 허가 승인을 획득했다고 30일 밝혔다.
이로써 스카이코비원은 영국에서 8번째로 정식 승인을 받은 코로나19 백신이 됐다. 스카이코비원은 지난해 3월부터 MHRA의 신속 승인을 위한 순차심사(Rolling Review)를 진행해왔으며, 임상 3상 결과를 바탕으로 만 1년 2개월 만에 정식 허가 승인을 받았다.
영국은 미국 FDA, 유럽 EMA 등과 더불어 의약품 승인에 까다로운 국가로, 국내에서 후보물질 발굴부터 임상까지 전 과정을 자체적으로 수행해 MHRA 승인을 받은 경우는 이례적이다.
SK바이오사이언스는 앞으로 WHO 긴급사용목록(Emergency Use Listing, EUL) 등재, 유럽의약품청(EMA) 판매 허가 등을 추가 획득해 코로나19 엔데믹 시대의 방역을 주도하겠다는 목표다. 실제로 미국, 일본, 호주 등에서 코로나19 백신 연례 접종에 대한 논의가 이어지고 있으며, 한국 정부도 코로나19 백신을 독감(인플루엔자) 백신처럼 연1회 접종하겠다고 밝힌 바 있다.
코로나19 백신이 연례접종화 될 경우 스카이코비원은 일부 코로나19 백신과는 다른 강점으로 시장 경쟁력을 가질 것으로 보인다. 일부 코로나19 백신의 경우 고가의 초저온설비를 필요로 하지만, 스카이코비원에 적용된 합성항원 방식은 냉장조건(2~8도)에서 보관 및 유통이 가능해 초저온설비를 갖추지 못한 중저개발국 시장에서 활용될 수 있다.
안재용 SK바이오사이언스 사장은 "어려운 상황에서도 서로를 믿고 노력해준 임직원에 감사하며, 이번 승인이 엔데믹 전환이라는 새로운 국면에서 우리의 글로벌 시장 입지를 굳힐 모멘텀이 될 것이라 확신한다"고 말했다.
hello@newspim.com
 영상
영상