[세종=뉴스핌] 신도경 기자 = 의약품과 의약외품 총 61개 품목이 신약‧자료제출 의약품‧안전성 심사 대상으로 허가됐다.
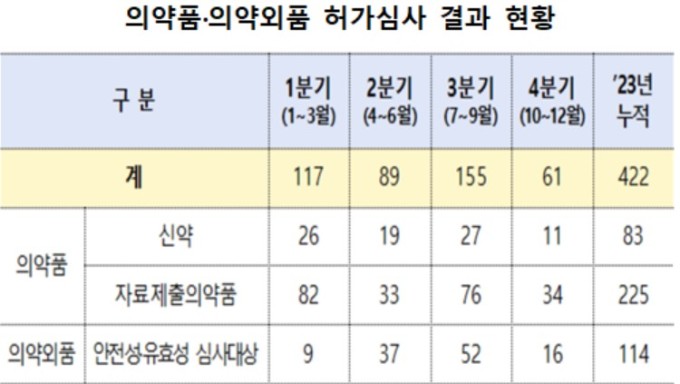
식품의약품안전처는 9일 '23년 4분기에 의약품 45개, 의약외품 16개 총 61개 품목의 허가심사 결과(허가보고서)를 공개했다.
작년 4분기에 허가된 신약은 총 11개다. 간세포암 치료제인 이뮤도주(트레멜리무맙)과 자가면역용혈성빈혈인 응집소병 치료제 엔제이모주(수팀리맙)이 있다. 전신 농포성 건선 치료제인 스페비고주(스페솔리맙), 경구용 코로나19 치료제 팍스로비드 정(니르마트렐비르, 리토나비르) 등도 포함됐다.
자료제출의약품은 34개다. 한미약품의 오메스트연질캡슐5/1000mg, 씨엘팜의 슬리필구강붕해필름(독시라민숙신산염) 등이 허가됐다. 산성-스핑고미엘린 분해효소 결핍증의 치료제인 젠포자임주(올리푸다제알파), 다발골수종 치료제 텍베일리주30·153mg(테클리스타맙)은 희귀의약품으로 허가됐다.
아모레퍼시픽의 엠씨이치약과 메디안브라운치약은 안전성과 유효성의 심사대상이 됐다. 주식회사피앤엘이 제조한 카오스비말차단마스크, 중원주식회사의 생리대 등을 포함해 16개가 의약외품 심사 대상으로 허가됐다.
식약처는 "의약품과 의약외품의 허가심사 결과를 공개해 제약업계의 제품 연구·개발에 도움이 되도록 할 것"이라고 밝혔다.
sdk1991@newspim.com
 영상
영상