[세종=뉴스핌] 임은석 기자 = 혈당측정기를 비롯해 안전성 우려가 적은 의료기기 시장 진출에 걸리는 시간이 확 줄어든다.
문재인 대통령은 19일 분당서울대병원에서 '혁신성장 확산을 위한 의료기기 분야 규제혁신 및 산업육성 방안'을 발표했다.
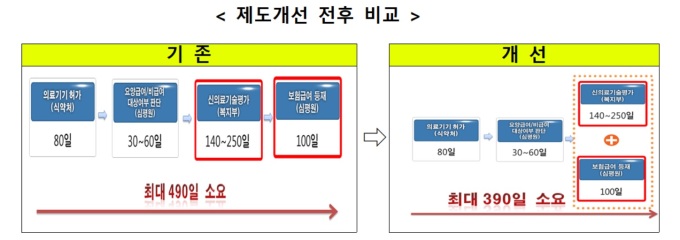
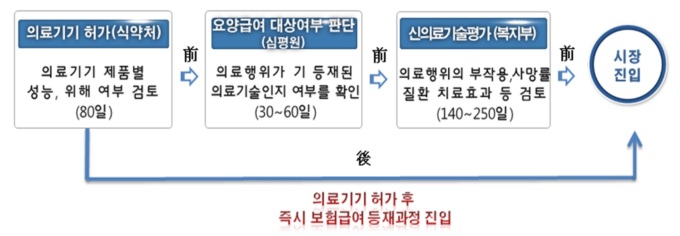
정부는 우선 기업체 등에서 개발한 신의료기술평가에 걸리는 시간을 280일에서 250일로 30일 단축한다. 또 보험등재심사와 신의료기술평가를 동시에 진행해 490일이나 걸리던 소요기간을 390일로 100일 줄이는 방안을 마련할 계획이다.
의료기기허가·신의료기술평가 등 통합심사는 '통합심사 전담팀'을 구성, 신청인과의 창구를 선임책임담당자로 일원화해 중복 자료요청 혼선을 없애고, 통합운영 심사시스템으로 자료를 공유할 계획이다.
통합운영 심사시스템은 실시간 심사자료 공유, 심사단계별 진행상황 자동알림, 평가별 분석데이터 제공 등의 기능을 제공하는 시스템으로, 지난 4월부터 가동에 들어갔다.
특히, 정부는 인체 안전성 우려가 적은 의료기기의 경우 '선 진입-후 평가' 방식으로 진입장벽을 확 낮추기로 했다.
업계의 요청이 많았던 체외진단검사분야 신의료기술평가를 사전평가에서 사후평가로 전환해 1년 넘게(390일) 걸리던 체외진단기기의 시장진입을 80일 이내로 대폭 단축할 예정이다.
체외진단기기는 신체 외부에서 사용하는 의료기기로, 연속혈당측정기와 인슐린펌프, 체온계 등이 대표적이다.
또, 체외진단기기가 기존 기기와 비교해 경미한 변경사항만 있을 경우 60일 가량 소요되던 식약처 변경허가를 면제한다.
규제과정의 그레이존(예측 불가능성) 해소를 위한 방안도 마련한다. 보건복지부, 식품의약품안전처, 건강보험심사평가원 등 의료기기 규제관련기관의 개별적 정보제공과 규제과정의 참여제한 등을 해소하기 위해 '의료기기산업 종합지원센터' 기능을 강화하고, 의료기기 규제절차에 대한 전 주기 통합상담을 실시한다.
규제정보 등에 대한 접근성을 높이기 위해 각 규제기관별 홈페이지와 연동되는 '통합정보포탈 시스템'도 구축할 계획이다.
규제과정의 투명성을 높이기 위해 관련 협회 등의 추천을 받은 혁신·첨단기술 전문가를 신의료기술평가위원회와 소위원회 등의 평가위원으로 위촉하고, 심사 문헌범위, 심사기준, 평가결과를 공개하는 절차를 복지부 고시에 규정하기로 했다.
아울러, 개발이력이 짧고 연구결과가 부족해 신의료기술평가에서 탈락하던 혁신·첨단 의료기술이 신속하게 시장에 진입할 수 있도록 하는 방안을 마련한다.
이를 위해 식약처는 혁신·첨단의료기기가 개발과 동시에 허가되도록하는 '신속허가 가이드라인'을 구축하고, 복지부는 연구결과 축적이 어려운 혁신·첨단 의료기술의 특성을 고려해 문헌적 근거가 다소 부족하더라도 잠재가치를 판단해 시장 진입을 허용하는 별도 평가트랙을 운용한다.
심평원은 의료진의 편의·생산성을 증진시키는 의료기술에 대해 예비분류 코드 혹은 확인증을 발급해 신의료기술평가 없이 시장에 진입할 수 있도록 하고, 기술혁신·개량 치료재료에 대한 가치 평가제도 개선으로 적정 보상체계를 마련할 계획이다.
문재인 대통령은 "의료기기 분야는 국민의 생명과 직결되는 분야"라며 "국민의 안전을 최우선으로 고려하면서 규제를 혁신해 나갈 것"이라고 말했다.
fedor01@newspim.com
 영상
영상