[세종=뉴스핌] 이경화 기자 = 지난해 국내승인 임상시험 건수는 전년보다 5.4% 늘어난 842건을 기록, 최근 3년간 꾸준히 증가한 것으로 나타났다. 제약사 주도 임상이 늘면서 전체 임상 건수 확대에 영향을 끼쳤다는 분석이다. 코로나19 백신·치료제, 항암제 등 국내개발 의약품의 다국적 임상이 크게 증가했다.
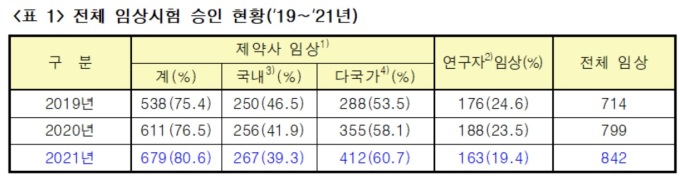
28일 식품의약품안전처와 국가임상시험지원재단이 공개한 '2021년 의약품 임상시험 승인 현황'에 따르면 연도별 임상시험 승인 건수는 2019년 714건, 2020년 799건, 2021년 842건으로 최근 3년간 꾸준히 늘어나는 추세다.
지난해 기준 전체 임상시험 중에서 제약사가 의약품 개발을 위해 수행하는 임상이 679건으로 80.6%를 차지했다. 제약사 주도 임상이 2020년 616건 대비 11.1% 증가하면서 전체 임상 승인 건수 확대를 이끌었다.
지난해 제약사가 의약품 개발을 위해 하는 임상 679건 중 다국가 임상이 412건(60.7%)으로 2020년 355건 대비 16.1% 늘었다. 무엇보다 다국가 임상 중에서 원 개발자가 국내 제약사인 경우가 27건(6.6%)으로 2020년 15건(4.2%)보다 증가했다.
이는 국내 제약사들이 코로나19 백신과 치료제, 항암제 등을 개발할 때 다국가 임상을 추진하는 경우가 많아졌기 때문으로 풀이된다. 다국가 임상에서는 1·2상 등 초기 임상의 비중(53.4%)이 3상 후기임상의 비중(43.7%)을 앞섰다.
임상을 효능별로 살펴보면 호흡기계(36건)와 심혈관계(90건)가 2020년 대비 각각 111.8%와 50.0% 증가했다. 효능별 전체 순위는 항암제(321건), 심혈관계(90건), 내분비계(62건), 감염병(항생제)(60건) 등 순이었다.
지난해 코로나19 치료제·백신 임상은 32건으로 파악됐다. 코로나19 상황이 지속된 데 따라 관련 임상도 2020년 37건과 유사한 수준으로 수행된 것이다. 지난해 국내 임상의 글로벌 순위는 6위로 2020년과 동일했다.
국가임상시험지원재단 관계자는 "앞으로 신·변종 감염병 대비는 물론 암·희귀질환 치료제 개발을 위한 공익적 임상시험 지원을 강화 하겠다"고 밝혔다.
식약처 관계자는 "임상시험 지원과 함께 임상시험 참여자 권익 보호와 안전관리 강화에도 적극 노력할 것"이라며 "최근의 감염병 유행으로 대면 임상시험이 어려운 임상시험의 환경변화 등에도 유연하게 대응하기 위해 제도개선을 선제적이고 지속적으로 추진하겠다"고 했다.
kh99@newspim.com
 영상
영상